O2PtF6称为六氟合铂酸氧,其中F是-1价,Pt是+5价,两个O原子团整体是+1价,他的键级经计算为2.5,验证了阳离子稳定性很强。电子转移是氧分子失一个电子给六氟合铂酸中的铂。这是人类第一次制得O正价的盐,证明PtF6是能够氧化氧分子的强氧化剂。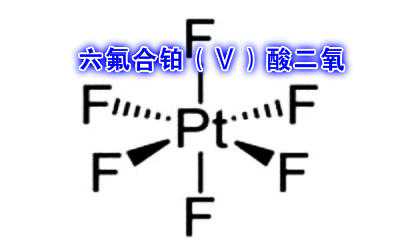
(六氟合铂酸氧中六氟合铂酸阴离子)
但是其被发现的最大意义在于引出稀有气体化合物的出现。因为在19世纪但是和稀有气体有什么关系?巴特列特头脑机敏,善于联想类比和推理。他考虑到O2的第一电离能是1175.7千焦/摩尔,氙的第一电离能是1175.5千焦/摩尔,比氧分子的第一电离能还略低,既然O2可以被PtF6氧化,那么氙也应能被PtF6氧化。接着将PtF6的蒸气与等摩尔的氙混合,在室温下竟然轻而易举地得到了一种橙黄色固体XePtF6,由于其室温下稳定,不溶于有机溶剂,进而确认了它是离子化合物。

(第一种稀有气体盐)
这样,具有历史意义的第一个含有化学键的“惰性”气体化合物诞生了。化学家们开始改变了原来的观念,摘掉了冠以稀有气体头上名不副实的“惰性”的帽子,很快形成了一个合成和研究新的稀有气体化合物的热潮,开辟了一个稀有气体化学的新天地。
(氙光)